Il forame ovale pervio (PFO) è la condizione in cui l’apertura del forame ovale, che dovrebbe chiudersi dopo la nascita tra l’atrio destro e l’atrio sinistro del cuore, rimane aperta. Questa apertura anatomica può essere asintomatica in alcuni individui, ma può essere associata a quadri clinici come embolia paradossa e ictus.
I sintomi del forame ovale pervio non sono evidenti nella maggior parte dei pazienti e spesso vengono rilevati incidentalmente. Tuttavia, il sospetto clinico aumenta nelle persone con anamnesi di ictus criptogenetico, emicrania con aura, attacco ischemico transitorio e raramente embolia sistemica. I reperti possono variare in base ai fattori di rischio cardiovascolare associati.
La diagnosi di forame ovale pervio viene posta mediante ecocardiografia transtoracica e soprattutto ecocardiografia transesofagea con contrasto. Il metodo noto come bubble test offre un’elevata sensibilità nel dimostrare la presenza di uno shunt destro-sinistro. Anche le valutazioni neurologiche sono importanti nel processo diagnostico.
Il trattamento del forame ovale pervio viene pianificato in base alle condizioni cliniche del paziente e al profilo di rischio embolico. Mentre nei casi asintomatici può essere sufficiente il follow-up, in pazienti selezionati con anamnesi di ictus può essere applicata la chiusura percutanea. La terapia antipiastrinica o anticoagulante viene regolata in base alla valutazione individuale del rischio.
Cose da sapere | Informazione |
Definizione | Il Forame Ovale Pervio (PFO) è la condizione in cui l’apertura intracardiaca chiamata forame ovale, che normalmente dovrebbe chiudersi dopo la nascita, rimane aperta. Il forame ovale è un’apertura fisiologica che durante la vita intrauterina consente al sangue di bypassare i polmoni ed entrare nella circolazione. |
Origine embriologica | Durante il periodo fetale, il forame ovale situato tra l’atrio destro e quello sinistro si chiude funzionalmente dopo la nascita a causa dell’aumento della pressione nell’atrio sinistro con l’inizio della circolazione polmonare. In alcuni individui questa chiusura non avviene completamente. |
Frequenza | Il PFO può essere presente in circa il 20–25% della popolazione. Nella maggior parte dei casi è asintomatico e viene rilevato incidentalmente. |
Fisiopatologia | In presenza di PFO, può formarsi uno shunt destro-sinistro transitorio o permanente dall’atrio destro all’atrio sinistro. Questa condizione diventa particolarmente evidente nelle situazioni in cui aumenta la pressione intratoracica (ad esempio, manovra di Valsalva). |
Importanza clinica | Nella maggior parte degli individui non provoca sintomi clinici. Tuttavia, in alcuni casi può essere associato a embolia paradossa, ictus criptogenetico ed eventi embolici sistemici. |
Relazione con i fattori di rischio | Il PFO può essere rilevato più frequentemente soprattutto nei pazienti giovani che hanno avuto un ictus inspiegato (criptogenetico). Inoltre, può aumentare il rischio di malattia da decompressione. |
Sintomi | Di solito non provoca sintomi. Nei possibili casi, può essere associato a sintomi di ictus (improvviso disturbo del linguaggio, perdita di forza), attacco ischemico transitorio o raramente emicrania. |
Metodi diagnostici | Per la diagnosi vengono utilizzati ecocardiografia transtoracica (TTE), ecocardiografia transesofagea (TEE) e bubble test (studio con contrasto salino). La TEE è più sensibile nella diagnosi del PFO. |
Opzioni di trattamento | Nella maggior parte dei casi asintomatici non è necessario alcun trattamento. Nei pazienti selezionati con anamnesi di ictus, si può prendere in considerazione una terapia medica (antipiastrinica o anticoagulante) o una chiusura percutanea. |
Prognosi | Nella maggior parte degli individui decorre senza problemi per tutta la vita. Nei pazienti che non hanno sviluppato eventi clinici, la prognosi è generalmente buona. |

Prof. Dr. Kadriye Kılıçkesmez
Cardiologia, Cardiologa interventista – Interventional Cardiologist
Prof. Dr. Kadriye Orta Kılıçkesmez è una delle figure di spicco nel campo della cardiologia in Turchia. È nata il 24 gennaio 1974 a Tekirdağ. Dopo aver completato la sua formazione universitaria presso la Facoltà di Medicina Cerrahpaşa dell'Università di Istanbul, ha scelto la cardiologia come specializzazione e ha ricevuto la sua formazione specialistica presso l'Istituto di Cardiologia della stessa università.
Dopo aver lavorato per un breve periodo presso l'Ospedale Statale di Çorlu e l'Ospedale di Servizio della Fondazione Turca del Rene, è tornata all'Istituto di Cardiologia dell'Università di Istanbul. Kadriye Kılıçkesmez, che ha proseguito qui la sua carriera accademica, è diventata professoressa associata nel 2012. Successivamente ha lavorato al Royal Brompton su interventi coronarici complessi, imaging intracoronarico CTO e malattie cardiache strutturali, e ha scritto articoli scientifici. Nel 2015, incaricata dall'università, ha fondato la clinica di cardiologia e il laboratorio di angiografia dello Şişli Etfal. Divenuta professoressa nel 2017, Kadriye Kılıçkesmez ha fondato nel 2020 la clinica di cardiologia e il laboratorio di angiografia dell'Ospedale Prof. Dr. Cemil Taşçıoğlu e ha garantito che la clinica diventasse una clinica di formazione.
Visualizza di piùChe cos’è il Forame Ovale Pervio (PFO)?
Il Forame Ovale Pervio (PFO) è la condizione in cui un’apertura nota come finestra ovale tra gli atri cardiaci non si chiude dopo la nascita. Normalmente, questa apertura, che durante la vita intrauterina consente a una parte del sangue del bambino di passare dal lato destro a quello sinistro del cuore senza andare ai polmoni, di solito si chiude dopo la nascita quando i polmoni iniziano a funzionare. Tuttavia, in alcuni individui questa chiusura non avviene e questa condizione chiamata PFO persiste. Questa apertura è presente mediamente nel 25–30% della popolazione adulta. Il PFO è generalmente una condizione asintomatica (che non provoca sintomi), e molte persone possono vivere per tutta la vita senza rendersene conto. Tuttavia, in alcuni casi può portare a gravi complicanze, soprattutto quando coaguli di sangue attraversano questa apertura e raggiungono il cervello o altri organi. Per questo motivo, comprendere il PFO e conoscerne i potenziali rischi è di grande importanza.
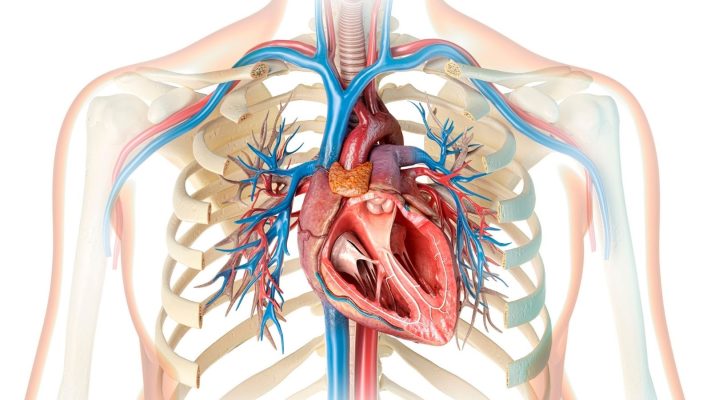
- Struttura del cuore e circolazione fetale
Il cuore è un organo complesso costituito da quattro camere: atrio destro, ventricolo destro, atrio sinistro e ventricolo sinistro. Il sangue ritorna dal corpo all’atrio destro, viene pompato ai polmoni dal ventricolo destro, qui si ossigena e ritorna all’atrio sinistro. Dal ventricolo sinistro viene poi pompato al resto del corpo. Nei bambini nel grembo materno, invece, poiché i polmoni non funzionano ancora, è necessario che il sangue ossigenato si mescoli con quello proveniente dalla placenta e si distribuisca al corpo. In questo processo, un’apertura chiamata Forame Ovale consente il passaggio diretto dall’atrio destro al sangue ossigenato presente nell’atrio sinistro. Inoltre, tra l’arteria polmonare e l’aorta esiste anche una connessione chiamata Dotto Arterioso. Con la nascita e l’inizio della respirazione polmonare, ci si aspetta che queste aperture si chiudano. La mancata chiusura del Forame Ovale è il PFO.
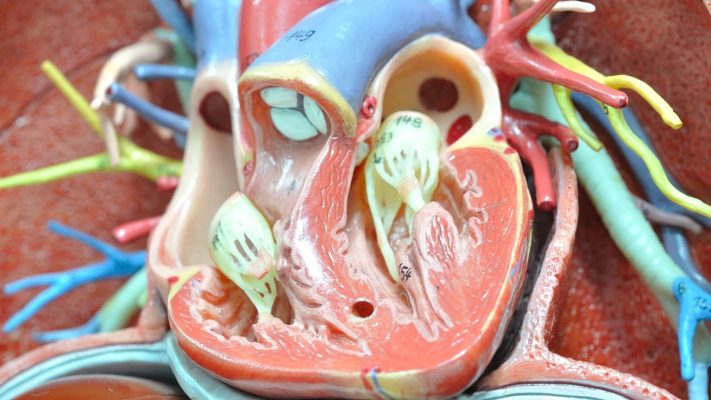
- Caratteristiche anatomiche del PFO
Il PFO si forma come conseguenza della mancata completa fusione delle pareti tra i due atri, chiamate septum primum e septum secundum. Questa apertura svolge generalmente il ruolo di un ponte tra l’atrio sinistro e l’atrio destro. Le dimensioni dell’apertura possono variare da persona a persona; alcune possono essere di pochi millimetri, altre di diversi millimetri di diametro. La presenza di questa apertura consente al sangue di mescolarsi, passando dall’atrio destro al sangue ossigenato dell’atrio sinistro. Questa condizione diventa più evidente soprattutto quando la pressione dell’atrio destro è superiore a quella dell’atrio sinistro (ad esempio mentre si tossisce, si starnutisce o si compie uno sforzo). La presenza del PFO da sola potrebbe non costituire un problema, ma i rischi possono aumentare quando si associa ad altre patologie cardiache sottostanti o a una tendenza alla coagulazione del sangue.
Cause del PFO: È una condizione congenita?
Il PFO è fondamentalmente un tipo di difetto cardiaco congenito, e si ritiene che si sviluppi come risultato della combinazione di predisposizione genetica e fattori dello sviluppo. La mancata chiusura di questa apertura durante la circolazione fetale nel grembo materno è la principale causa del PFO. Tuttavia, i motivi per cui questa chiusura non avviene non sono sempre chiaramente definiti. Alcune ricerche mostrano che determinate mutazioni genetiche possono aumentare il rischio di sviluppo del PFO. Inoltre, alcune infezioni della madre durante la gravidanza o i farmaci assunti possono influenzare indirettamente questo processo, anche se le prove definitive su questo punto sono limitate. La maggior parte dei casi di PFO si sviluppa spontaneamente senza un fattore scatenante specifico. Nella formazione di questa condizione, giocano un ruolo la struttura complessa del sistema circolatorio nel grembo materno e il mancato completo verificarsi dei cambiamenti fisiologici dopo la nascita. Nello sviluppo del PFO, piccole deviazioni nel processo di sviluppo embriologico risultano più determinanti dei fattori ambientali.
- Il ruolo dei fattori genetici
La genetica è un fattore importante che può svolgere un ruolo nello sviluppo del PFO. Negli individui con una storia familiare di PFO, la probabilità di manifestare questa condizione è più elevata. Tuttavia, il modello di ereditarietà del PFO non è stato completamente chiarito; cioè, non si può dire che sia responsabile un solo gene. Si ritiene che possa emergere come risultato dell’interazione di più geni oppure della combinazione tra predisposizione genetica e fattori ambientali. Alcuni studi hanno indagato variazioni genetiche che potrebbero essere associate al PFO, ma in questo campo sono necessarie ulteriori ricerche. La predisposizione genetica può portare ad anomalie nel meccanismo di chiusura dell’apertura o a piccoli difetti nello sviluppo delle pareti cardiache. Per questo motivo, si raccomanda cautela alle persone con una storia familiare di PFO o di condizioni correlate (ad esempio ictus).
- Anomalie nel processo di sviluppo fetale
Durante lo sviluppo del bambino nel grembo materno, la formazione del cuore e dei grandi vasi è un processo estremamente complesso. Anche la chiusura del Forame Ovale fa parte di questo processo. Se durante questo processo di chiusura si verifica un’alterazione, può formarsi un PFO. Le cause di queste alterazioni possono essere varie; per esempio, piccoli errori durante la migrazione o la fusione cellulare, fattori genetici o alcuni fattori ambientali nel grembo materno possono influenzare questo processo. Tuttavia, nella maggior parte dei casi di PFO non viene identificato un chiaro fattore teratogeno (che altera lo sviluppo). Questo porta a considerare il PFO generalmente come un’anomalia dello sviluppo casuale. Queste piccole deviazioni nel meccanismo di chiusura impediscono che l’apertura si chiuda spontaneamente dopo la nascita.
Sintomi del PFO: Per lo più rimane silenzioso
La caratteristica più evidente del PFO è che nella maggior parte dei casi non provoca alcun sintomo. Per questo motivo, molte persone vivono per tutta la vita senza rendersi conto di questa condizione. Tuttavia, in alcuni individui il PFO può causare problemi seri, soprattutto quando coaguli di sangue attraversano questa apertura e raggiungono il cervello. Quando si verificano tali complicanze, possono comparire sintomi. Il PFO in sé non provoca direttamente dolore o fastidio; i sintomi derivano generalmente da condizioni secondarie causate dal PFO. Per questo motivo, la diagnosi di PFO viene generalmente posta incidentalmente durante l’indagine di un’altra condizione medica.
- Relazione con l’ictus (evento cerebrovascolare)
Una delle complicanze più importanti e temute associate al PFO è l’ictus. In particolare, viene studiato il ruolo del PFO negli ictus che si verificano in persone giovani (sotto i 55 anni) e senza fattori di rischio noti (come ipertensione, diabete, colesterolo alto). Il PFO può causare il passaggio di un coagulo di sangue formatosi in qualsiasi parte del corpo (generalmente una trombosi venosa profonda – TVP – nelle gambe) dal lato destro al lato sinistro del cuore e quindi l’ostruzione dei vasi cerebrali. Questa condizione è chiamata embolia paradossa. Tra i sintomi dell’ictus vi sono improvviso disturbo del linguaggio, debolezza o intorpidimento di viso, braccio o gamba (generalmente su un solo lato del corpo), perdita della vista, perdita dell’equilibrio e forte mal di testa. Questi sintomi richiedono un intervento medico urgente.
- Emicrania e PFO
Le ricerche condotte negli ultimi anni hanno portato all’attenzione la possibile relazione tra PFO ed emicrania. In particolare, è stato rilevato che il PFO è più frequente nei tipi di emicrania noti come emicrania con aura, accompagnati da disturbi visivi, uditivi o sensoriali che compaiono prima dell’attacco emicranico. Esistono diverse teorie secondo cui il PFO potrebbe scatenare gli attacchi di emicrania. Una di queste è che alcune sostanze (ad esempio neuropeptidi) che passano dall’atrio destro al sangue ossigenato dell’atrio sinistro influenzino i vasi sanguigni del cervello e inneschino l’emicrania. Un’altra teoria è che il PFO alteri il flusso del sangue venoso di ritorno dal cervello, aumentando il dolore emicranico. La presenza di PFO nei pazienti con emicrania viene valutata come opzione nei casi di emicrania resistente al trattamento.
Metodi diagnostici del PFO: Raggiungere una diagnosi certa
La diagnosi del PFO viene posta attraverso l’uso combinato dell’anamnesi medica del paziente, dei reperti dell’esame obiettivo e di vari metodi di imaging. Poiché i sintomi sono generalmente indiretti, è importante identificare direttamente il PFO stesso. Questo processo diagnostico inizia di solito durante l’indagine di ictus, emicrania o altre condizioni sospette. I medici prendono in considerazione la possibilità di un PFO valutando attentamente i fattori di rischio e i sintomi del paziente. I principali metodi diagnostici utilizzati sono i seguenti:
- Ecocardiografia (ECO)
L’ecocardiografia è il metodo più frequentemente utilizzato nella diagnosi del PFO. Questo metodo consente di visualizzare in dettaglio la struttura del cuore, le sue camere, le valvole e il flusso sanguigno utilizzando onde ultrasonore. Per rilevare la presenza di PFO, si preferisce generalmente l’ecocardiografia transesofagea (TEE). Nella TEE, una sonda sottile e flessibile viene inserita nell’esofago per ottenere immagini ad alta risoluzione da una posizione più vicina al cuore. Durante questo esame, al paziente viene somministrato per via endovenosa un colorante speciale (mezzo di contrasto). Se è presente un PFO, si osserva il passaggio di queste bolle colorate dall’atrio destro al sangue ossigenato dell’atrio sinistro. Questo reperto conferma in modo definitivo la presenza del PFO. Può essere utilizzata anche l’ecocardiografia transtoracica (ECO eseguita attraverso la parete toracica), ma non è sensibile quanto la TEE nel rilevare il PFO.
- Ecografia Doppler transcranica (TCD) e manovra di Valsalva
L’ecografia Doppler transcranica (TCD) è un metodo utilizzato per valutare il flusso sanguigno nei vasi cerebrali. Nella diagnosi del PFO, il TCD viene generalmente utilizzato insieme all’ecocardiografia. Con questo metodo, al paziente viene chiesto di eseguire la manovra di Valsalva. La manovra di Valsalva consiste nel trattenere il respiro e spingere. Durante questa manovra, aumenta la pressione intra-addominale e questo aumenta la pressione sul lato destro del cuore. Se è presente un PFO, a causa di questo aumento di pressione aumenta il passaggio del sangue dall’atrio destro al sangue ossigenato dell’atrio sinistro. In questo momento, il mezzo di contrasto somministrato per via endovenosa può essere rilevato nei vasi cerebrali con il dispositivo TCD. La sensibilità del TCD è elevata e svolge un ruolo importante soprattutto nel rilevamento del PFO nei pazienti a rischio di ictus. Questo metodo aiuta a valutare il potenziale del PFO di inviare coaguli al cervello.
- Risonanza magnetica cardiaca (RM cardiaca) e tomografia computerizzata (TC)
Tecniche di imaging avanzate come la risonanza magnetica (RM) cardiaca e la tomografia computerizzata (TC) possono essere utilizzate anche nella diagnosi del PFO. La RM cardiaca offre immagini ad alta risoluzione della struttura anatomica dettagliata e delle funzioni del cuore. È particolarmente utile per valutare le dimensioni, la forma del PFO e altre anomalie cardiache associate. L’angio-TC, invece, può essere utilizzata per visualizzare più chiaramente i vasi cardiaci e l’apertura del PFO. Questi metodi possono essere preferiti soprattutto nei casi in cui l’ecocardiografia non fornisca un risultato chiaro oppure prima della pianificazione di un trattamento chirurgico. Tuttavia, questi metodi possono essere generalmente più costosi e meno accessibili rispetto all’ecocardiografia. Inoltre, la TC comporta esposizione alle radiazioni.
Trattamento del PFO: Un percorso che va dall’osservazione alla chirurgia
Il trattamento del PFO viene determinato in base all’età del paziente, alla gravità dei sintomi, alle dimensioni del PFO e allo stato generale di salute del paziente. Non tutti i casi di PFO richiedono trattamento. Per molte persone possono essere sufficienti un monitoraggio regolare e l’osservazione. Tuttavia, se il PFO provoca gravi complicanze (ad esempio ictus, attacchi ricorrenti di emicrania), vengono valutate le opzioni terapeutiche. Gli approcci terapeutici possono includere terapia farmacologica, metodi minimamente invasivi e raramente intervento chirurgico. I medici elaborano il piano terapeutico più appropriato valutando attentamente i fattori di rischio individuali del paziente e il rapporto rischio-beneficio.
- Terapia farmacologica e cambiamenti dello stile di vita
Non esiste una terapia farmacologica specifica per il PFO in sé. Tuttavia, possono essere prescritti farmaci fluidificanti del sangue (antipiastrinici o anticoagulanti) per prevenire le complicanze associate al PFO. Soprattutto nei pazienti che hanno avuto un ictus, questi farmaci vengono utilizzati per impedire la formazione di nuovi coaguli e prevenire che i coaguli raggiungano il cervello. Aspirina, clopidogrel, warfarin oppure agenti anticoagulanti di nuova generazione vengono utilizzati su indicazione del medico. Inoltre, anche i cambiamenti dello stile di vita sono importanti. Misure come alimentazione sana, esercizio fisico regolare, smettere di fumare, limitare il consumo di alcol e controllo del peso migliorano la salute cardiaca generale e riducono il rischio di possibili complicanze. Queste misure diventano ancora più importanti soprattutto nei pazienti con tendenza alla coagulazione del sangue.
- Metodi di chiusura percutanea (chiusura con dispositivo)
La chiusura percutanea è il metodo minimamente invasivo più frequentemente applicato nel trattamento del PFO. In questo metodo, senza incisione chirurgica, l’apertura del PFO viene chiusa mediante uno speciale catetere introdotto dall’inguine. La procedura viene generalmente eseguita in laboratorio di angiografia e sotto anestesia locale. Per la chiusura si utilizzano dispositivi appositamente progettati simili a un ombrello. Questi dispositivi vengono posizionati nell’apertura del PFO con l’aiuto del catetere e chiudono l’apertura ancorandosi a entrambe le pareti atriali. Con il tempo, si sviluppa tessuto attorno a questo dispositivo e l’apertura si chiude in modo permanente. Il metodo di chiusura percutanea rappresenta un’opzione meno rischiosa per i pazienti, offre un processo di recupero più rapido e riduce la durata della degenza ospedaliera. Questo metodo viene applicato con successo soprattutto nei pazienti con ictus ricorrente o gravi attacchi di emicrania. In media ha un tasso di successo superiore al 90%.
- Chiusura chirurgica (riparazione del difetto del setto atriale)
La chiusura chirurgica è un metodo meno preferito nel trattamento del PFO, ma in alcuni casi può essere necessaria. Questo metodo viene generalmente applicato insieme ad altri interventi cardiaci o nei casi in cui la chiusura percutanea non sia possibile. La chiusura chirurgica può essere eseguita come chirurgia a cuore aperto. Viene aperta la gabbia toracica e il cuore viene riparato direttamente. Oggi si utilizzano anche tecniche chirurgiche più minimamente invasive; per esempio, il PFO può essere chiuso con chirurgia toracoscopica attraverso piccole incisioni. Nella riparazione chirurgica, l’apertura viene generalmente chiusa con suture o utilizzando una patch. Questo metodo può essere più adatto nei pazienti con strutture di PFO più complesse o con altri problemi cardiaci associati. Tuttavia, l’intervento chirurgico comporta un rischio maggiore rispetto ai metodi percutanei e il processo di recupero è più lungo.
Ultimi sviluppi nel trattamento del PFO e prospettive future
Il trattamento del PFO progredisce continuamente con lo sviluppo della tecnologia. La diffusione dei metodi minimamente invasivi e lo sviluppo di nuovi dispositivi offrono ai pazienti opzioni terapeutiche più sicure ed efficaci. In futuro, si prevede che gli approcci di medicina personalizzata acquisiranno ancora maggiore importanza nel trattamento del PFO. Grazie alle analisi genetiche e alle tecniche di imaging avanzate, le caratteristiche specifiche del PFO di ciascun paziente saranno comprese meglio e i piani terapeutici verranno ottimizzati di conseguenza. Inoltre, una migliore comprensione di altre condizioni associate al PFO (ad esempio emicrania, apnea del sonno) e la loro integrazione con il trattamento del PFO rappresentano un altro importante campo di ricerca futuro. Gli scienziati stanno lavorando a dispositivi di chiusura ancora più avanzati e a metodi diagnostici più sensibili.
- Dispositivi di chiusura di nuova generazione
I dispositivi utilizzati nei metodi di chiusura percutanea vengono continuamente sviluppati. I dispositivi di nuova generazione sono realizzati con materiali più biocompatibili, possono essere posizionati più facilmente e integrarsi meglio con i tessuti. Il design di questi dispositivi si concentra sulla riduzione del rischio di complicanze come trombosi (formazione di coaguli) e aritmia (disturbo del ritmo cardiaco). Alcuni nuovi dispositivi presentano una struttura più flessibile e adattabile per garantire la chiusura completa dell’apertura del PFO. Inoltre, aumentando la varietà delle dimensioni dei dispositivi, vengono offerte soluzioni più adatte a diverse dimensioni e anatomie del PFO. Questi sviluppi rendono possibile trattare più pazienti senza necessità di chirurgia. Per esempio, alcuni dispositivi sono realizzati con metalli flessibili e a memoria di forma come il nitinol (lega nichel-titanio), e questo facilita la procedura di posizionamento.
- Approcci terapeutici personalizzati
Gli approcci personalizzati nel trattamento del PFO indicano la definizione del piano terapeutico considerando la struttura genetica del paziente, il suo stile di vita, le malattie concomitanti e le caratteristiche specifiche del PFO. Per esempio, nei pazienti con elevata predisposizione genetica possono essere adottate strategie terapeutiche più aggressive, mentre nei pazienti a basso rischio può essere preferita l’osservazione. L’ecocardiografia 3D e le tecniche avanzate di RM mostrano in modo molto più dettagliato le caratteristiche anatomiche del PFO e aiutano a selezionare il dispositivo di chiusura più adatto. Inoltre, anche altre condizioni che influenzano la qualità della vita del paziente (ad esempio emicrania grave) vengono integrate nel piano terapeutico. Questo approccio mira ad aumentare il successo del trattamento evitando allo stesso tempo interventi inutili.
Effetto del PFO sulla qualità della vita e sua gestione
Il PFO di per sé generalmente non influisce direttamente sulla qualità della vita. Tuttavia, ictus, emicrania o altre complicanze che si sviluppano in relazione al PFO possono ridurre significativamente la qualità della vita. Per questo motivo, una gestione efficace del PFO e la prevenzione delle possibili complicanze sono di grande importanza. Controlli medici regolari, uso regolare dei farmaci raccomandati dal medico e adozione di sane abitudini di vita aiutano gli individui con PFO a condurre una vita di migliore qualità. È anche importante mantenere il livello di attività fisica, ma evitare attività troppo impegnative. Si raccomanda ai pazienti di essere consapevoli del proprio stato di salute e di consultare immediatamente il medico in caso di comparsa di nuovi sintomi.
- Follow-up del paziente e controlli medici
Dopo la diagnosi di PFO, il paziente deve essere seguito regolarmente dal proprio medico. La frequenza di questi controlli viene determinata in base alla condizione del paziente, alla sua età e all’eventuale presenza o assenza di complicanze associate al PFO. Durante i controlli medici vengono valutate le condizioni generali di salute del paziente, e vengono controllati la pressione arteriosa e i livelli di colesterolo. Se il paziente assume farmaci, vengono riesaminati l’efficacia dei farmaci e i possibili effetti collaterali. Inoltre, si indaga se il paziente abbia manifestato nuovi sintomi (ad esempio mal di testa, cambiamenti della vista, difficoltà di parola). Quando necessario, possono essere ripetuti metodi di imaging come l’ecocardiografia. Questo regolare processo di follow-up consente la diagnosi precoce di eventuali complicanze e un intervento tempestivo.
- Supporto psicologico e informazione
Vivere con una condizione cronica come il PFO può generare ansia e stress in alcuni individui. Soprattutto nelle situazioni che comportano il rischio di gravi complicanze come l’ictus, è importante fornire supporto psicologico ai pazienti. Il fatto che i pazienti dispongano di informazioni corrette e aggiornate sul PFO li aiuta a comprendere e gestire meglio la propria condizione. Medici di medicina generale, cardiologi e neurologi svolgono un ruolo importante nel rispondere alle domande dei pazienti e alleviare le loro preoccupazioni. Quando necessario, può essere fornito anche il supporto di psicologi o psichiatri. Anche i programmi educativi per i pazienti e i gruppi di sostegno consentono ai pazienti di condividere le proprie esperienze tra loro e di sentire di non essere soli. L’informazione incoraggia la partecipazione attiva del paziente al processo di trattamento.
Domande frequenti
Il PFO si forma quando il canale del forame ovale, aperto nel grembo materno, non si chiude completamente dopo la nascita. Questa apertura tra gli atri può consentire, durante i cambiamenti di pressione, il passaggio del sangue da destra a sinistra, preparando il terreno alla mescolanza di coaguli nella circolazione sistemica.
Il PFO è un fattore importante soprattutto nei casi di ictus inspiegabile nei giovani. Piccoli coaguli formatisi nelle vene delle gambe possono attraversare l’apertura nel cuore, occludere i vasi cerebrali e portare a un quadro chiamato “embolia paradossa”.
In alcuni studi, il PFO è stato rilevato più frequentemente soprattutto nelle persone con emicrania con aura. I microemboli che passano da destra a sinistra o il raggiungimento del cervello da parte di sostanze chimiche circolanti senza essere filtrate sono considerati tra i meccanismi che possono scatenare gli attacchi di emicrania.
L’aumentata tendenza alla coagulazione durante la gravidanza può teoricamente aumentare il rischio di ictus in presenza di PFO. Tuttavia, la maggior parte delle donne con PFO affronta una gravidanza senza problemi. Nelle situazioni ad alto rischio, è importante il follow-up congiunto da parte degli specialisti in ginecologia e cardiologia.
Le bolle di gas che si formano durante le immersioni subacquee normalmente vengono filtrate nei polmoni. In presenza di PFO, queste bolle possono passare al cervello e ad altri organi, causando un decorso più grave della malattia da decompressione.
Nei pazienti con ictus inspiegabili ricorrenti e senza altri fattori di rischio, i cardiologi possono raccomandare la chiusura del PFO. La decisione viene presa individualmente in base all’età, all’anamnesi di coaguli e alle caratteristiche anatomiche dell’apertura.
La procedura di chiusura eseguita attraverso l’inguine consente generalmente una dimissione in tempi brevi. I pazienti possono tornare alla vita quotidiana entro pochi giorni, ma sono necessari alcuni mesi di terapia fluidificante del sangue e controlli regolari affinché il dispositivo si stabilizzi completamente.
La maggior parte dei PFO non provoca sintomi per tutta la vita. Tuttavia, negli individui a rischio possono verificarsi ictus, attacco ischemico transitorio o raramente embolia sistemica. Per questo motivo, l’analisi del rischio personale e il regolare follow-up medico sono di grande importanza.
È importante non rimanere immobili per lunghi periodi, assumere una quantità sufficiente di liquidi ed evitare abitudini come il fumo che aumentano il rischio di coaguli. Durante i voli lunghi, l’uso di calze compressive e il movimento a intervalli possono essere protettivi.
Soprattutto quando viene rilevato dopo un ictus, il PFO può creare nel paziente un senso di ansia e incertezza. Una spiegazione dettagliata delle opzioni terapeutiche e un regolare piano di follow-up aiutano a ridurre il carico psicologico aumentando il senso di controllo del paziente.