La fermeture de l’ASD sans chirurgie est une procédure consistant à fermer la communication interauriculaire par méthode de cathéter, sans recourir à une chirurgie ouverte. Cette méthode permet une fermeture contrôlée de l’orifice dans le cœur à l’aide d’un dispositif spécial de fermeture avancé par la veine inguinale et offre, chez les patients appropriés, une option thérapeutique sûre.
La méthode de fermeture de l’ASD sans chirurgie est particulièrement privilégiée dans les communications interauriculaires de type secundum, et l’intervention est réalisée en laboratoire d’angiographie. Le dispositif, avancé sous fluoroscopie et échocardiographie, est placé dans la zone du défaut et assure une fermeture permanente en saisissant le septum des deux côtés grâce à sa structure à double disque.
Parmi les avantages de la fermeture de l’ASD par cathéter figurent une courte durée d’hospitalisation, l’absence de nécessité d’une anesthésie générale et un processus de récupération rapide. L’absence d’ouverture de la cage thoracique réduit le risque d’infection et de saignement, offre également un avantage esthétique marqué et raccourcit le délai de retour à la vie quotidienne.
Le processus de suivi après une fermeture de l’ASD sans chirurgie comprend des contrôles cardiologiques réguliers et la position du dispositif est surveillée par évaluation échocardiographique. Après l’intervention, un traitement antiplaquettaire est appliqué pendant une certaine période et le retour des patients à l’activité physique est planifié selon les recommandations du médecin.
Ce que vous devez savoir | Information |
Définition | La fermeture de l’ASD (défaut du septum interauriculaire) sans chirurgie est la procédure consistant à fermer, sans chirurgie à cœur ouvert, l’orifice situé entre les oreillettes droite et gauche du cœur (atriums), au moyen d’un cathéter et d’un dispositif spécial de fermeture. |
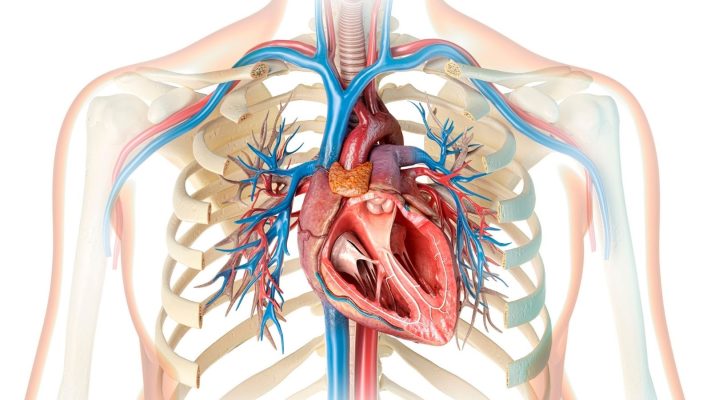
Qu’est-ce qu’un ASD ? | Le défaut du septum interauriculaire est une affection caractérisée par la présence d’une ouverture dans le septum entre les atriums, faisant partie des cardiopathies congénitales. Cette ouverture provoque le passage du sang oxygéné de l’oreillette gauche vers l’oreillette droite. |
Types d’ASD adaptés | Elle est le plus souvent appliquée dans les ASD de type secundum. Les ASD de type primum, de type sinus veineux et de type sinus coronaire nécessitent généralement un traitement chirurgical et ne sont pas adaptés à la méthode par cathéter. |
Indications | Elle est recommandée chez les patients présentant une dilatation des cavités cardiaques droites, la présence d’un shunt gauche-droite significatif, une intolérance à l’effort, une fatigabilité rapide, un essoufflement, des infections pulmonaires répétées et des antécédents d’embolie paradoxale. |
Pour qui n’est-ce pas adapté ? | Elle peut ne pas être adaptée en cas de défauts très volumineux, chez les patients ne présentant pas un tissu de bord septal suffisant, ou en présence d’une maladie valvulaire cardiaque sévère associée ou d’autres anomalies cardiaques nécessitant une chirurgie. |
Comment la procédure est-elle réalisée ? | On atteint généralement le cœur à l’aide d’un cathéter en passant par la veine fémorale au niveau de l’aine. Un dispositif spécial de fermeture à double disque est placé sur la zone du défaut et ferme l’orifice en s’attachant aux deux côtés du septum. |
Type d’anesthésie | Elle est le plus souvent réalisée sous anesthésie générale ou sédation profonde. Pendant la procédure, l’imagerie est effectuée par échocardiographie transœsophagienne (ETO) ou échocardiographie intracardiaque. |
Durée de la procédure | Elle dure en moyenne entre 30 et 90 minutes ; elle peut varier selon les caractéristiques anatomiques du patient. |
Durée d’hospitalisation | Une observation d’un jour à l’hôpital est généralement suffisante. En l’absence de complication, le patient peut sortir le lendemain. |
Avantages | Elle est moins invasive que la chirurgie à cœur ouvert, le sternum n’est pas sectionné, le temps de récupération est court, la douleur est moindre et le risque d’infection est plus faible. |
Risques possibles | Des complications telles que l’embolisation du dispositif, des troubles du rythme cardiaque, une lésion vasculaire, un épanchement péricardique, la formation de thrombus, un shunt résiduel et, plus rarement, une érosion du dispositif peuvent être observées. |
Taux de réussite | Lorsque la sélection des patients est appropriée, le taux de réussite est supérieur à 95 %. Les résultats à long terme sont généralement favorables. |
Suivi après la procédure | Des contrôles cardiologiques réguliers sont recommandés pendant les 6 premiers mois. La position du dispositif et la présence d’un shunt résiduel sont évaluées par échocardiographie. |
Utilisation de médicaments | Après la procédure, un traitement antiplaquettaire (par exemple l’acide acétylsalicylique) est généralement recommandé pendant 3 à 6 mois. Chez certains patients, un second médicament antiplaquettaire peut également être administré. |
Retour à la vie quotidienne | La plupart des patients peuvent reprendre leurs activités quotidiennes normales en quelques jours. Pour les activités physiques intenses, la durée est déterminée selon les recommandations du médecin. |
Pronostic à long terme | Après une fermeture réussie, la charge du cœur droit diminue, les symptômes régressent et la qualité de vie augmente. Les procédures de fermeture réalisées précocement réduisent le risque de complications à long terme. |

Prof. Dr. Kadriye Kılıçkesmez
Cardiologie, Cardiologue interventionnelle – Interventional Cardiologist
Prof. Dr. Kadriye Orta Kılıçkesmez est l'une des figures de proue du domaine de la cardiologie en Turquie. Elle est née le 24 janvier 1974 à Tekirdağ. Après avoir terminé ses études de licence à la Faculté de Médecine Cerrahpaşa de l'Université d'Istanbul, elle a choisi la cardiologie comme spécialité et a suivi sa formation de spécialisation à l'Institut de Cardiologie de la même université.
Après avoir travaillé pendant une courte période à l'Hôpital Public de Çorlu et à l'Hôpital de Service de la Fondation Turque du Rein, elle est retournée à l'Institut de Cardiologie de l'Université d'Istanbul. Kadriye Kılıçkesmez, qui a poursuivi sa carrière académique ici, est devenue professeure associée en 2012. Par la suite, elle a travaillé au Royal Brompton sur les interventions coronaires complexes, l'imagerie intracoronaire CTO et les maladies cardiaques structurelles, et a rédigé des articles scientifiques. En 2015, elle a été mandatée par l'université pour fonder la clinique de cardiologie de Şişli Etfal ainsi que le laboratoire d'angiographie. Devenue professeure en 2017, Kadriye Kılıçkesmez a fondé en 2020 la clinique de cardiologie et le laboratoire d'angiographie de l'Hôpital Prof. Dr. Cemil Taşçıoğlu et a assuré que la clinique devienne une clinique de formation.
Voir plusQu’est-ce que le défaut du septum interauriculaire (ASD) ?
Le défaut du septum interauriculaire (ASD) est une ouverture située dans le septum, la paroi entre les oreillettes (atriums) du cœur. Normalement, le sang non oxygéné qui revient dans l’oreillette droite du cœur et le sang oxygéné qui arrive dans l’oreillette gauche sont maintenus séparés. En présence d’un ASD, ces deux flux sanguins se mélangent. Ce mélange augmente la charge de travail du cœur et peut entraîner divers problèmes de santé à long terme.
Causes de l’ASD
La cause exacte de l’ASD est le plus souvent inconnue. Cependant, on pense que des facteurs tels que les facteurs génétiques, les infections pendant la grossesse ou l’exposition à certains tératogènes peuvent jouer un rôle. Dans certains cas, l’ASD peut présenter une transmission familiale. En outre, sa fréquence peut être plus élevée en association avec des anomalies génétiques telles que le syndrome de Down.
Types d’ASD
Les ASD sont classés selon leur localisation dans le septum et leur taille :
- ASD secundum : C’est le type le plus fréquent. Il se situe dans la partie moyenne du septum, c’est-à-dire dans la partie arrière des oreillettes.
- ASD primum : Il se trouve dans la partie inférieure du septum, dans une région proche des valves tricuspide et mitrale.
- ASD du sinus veineux : Il est situé près de la zone où la veine cave supérieure ou la veine cave inférieure entre dans l’oreillette.
- ASD du sinus coronaire : C’est un type rare qui comprend un défaut du sinus coronaire.
Symptômes de l’ASD
Les petits ASD peuvent généralement ne provoquer aucun symptôme et être diagnostiqués de façon fortuite. Cependant, les défauts plus grands ou ceux qui s’agrandissent avec le temps peuvent entraîner les symptômes suivants :
- Essoufflement : Ressenti en particulier à l’effort.
- Fatigue : Baisse du niveau d’énergie.
- Palpitations cardiaques : Battements cardiaques irréguliers.
- Infections respiratoires fréquentes : En particulier chez les enfants.
- Retard de croissance : Chez les nourrissons et les enfants.
- Accident vasculaire cérébral (paralysie) : Dans de rares cas, il peut survenir en raison du passage de caillots sanguins de la droite vers la gauche.
Diagnostic de l’ASD
Le diagnostic de l’ASD est généralement établi par des méthodes telles que l’examen physique, l’électrocardiographie (ECG), l’échocardiographie (ECHO) et plus rarement le cathétérisme cardiaque. Après avoir évalué vos symptômes et vos antécédents médicaux, votre médecin déterminera les méthodes diagnostiques appropriées.
- Échocardiographie (ECHO)
L’échocardiographie est la méthode la plus fréquemment utilisée dans le diagnostic de l’ASD. Elle visualise la structure, la taille du cœur et le flux sanguin à l’aide d’ondes ultrasonores. Elle permet ainsi d’obtenir des informations détaillées sur la localisation, la taille et la gravité du défaut.
- Échocardiographie transœsophagienne (ETO)
Dans certains cas, une échocardiographie réalisée par l’œsophage (ETO) peut être privilégiée afin d’obtenir des images plus nettes. Cette méthode permet une visualisation plus rapprochée et plus détaillée du cœur.
- Imagerie par résonance magnétique cardiaque (IRM) et tomodensitométrie (TDM)
Ces méthodes d’imagerie peuvent être utilisées pour fournir des informations supplémentaires, en particulier dans les cas complexes d’ASD ou au stade de la planification chirurgicale.
Traitement traditionnel de l’ASD : méthodes chirurgicales
Par le passé, le traitement de l’ASD reposait presque entièrement sur des méthodes chirurgicales. Lors d’une chirurgie à cœur ouvert, on accède au cœur en sectionnant le sternum (os de la poitrine), et l’orifice est fermé à l’aide de patchs spéciaux ou du propre tissu du cœur. Ces méthodes sont efficaces, mais elles signifiaient pour les patients un temps de récupération plus long, davantage de douleur et un risque plus élevé d’infection.
- Chirurgie à cœur ouvert
Dans cette méthode, le chirurgien ouvre la cage thoracique pour accéder directement au cœur. Selon la taille et la localisation de l’ASD, un patch synthétique ou du péricarde autologue (membrane du cœur) est utilisé. Le processus de récupération après la chirurgie dure généralement plusieurs semaines et le retour des patients à l’activité physique peut prendre du temps.
- Chirurgie minimalement invasive
Avec le développement de la technologie, des techniques chirurgicales minimalement invasives réalisées avec de plus petites incisions, au lieu d’ouvrir complètement la cage thoracique, ont également été développées. Ces méthodes peuvent raccourcir le temps de récupération et offrir de meilleurs résultats sur le plan esthétique. Cependant, elles nécessitent toujours une intervention chirurgicale.
Fermeture de l’ASD sans chirurgie : méthodes percutanées
Ces dernières années, les méthodes de fermeture de l’ASD sans chirurgie ont connu un grand développement. Ces méthodes relèvent du domaine de la cardiologie interventionnelle percutanée et sont généralement appliquées par l’ouverture d’un petit accès vasculaire au niveau de l’aine ou du cou. Ainsi, l’ASD peut être fermé sans qu’une chirurgie à cœur ouvert soit nécessaire.
Dispositifs de fermeture percutanée de l’ASD
Ces dispositifs, qui constituent la base de la fermeture de l’ASD sans chirurgie, sont des implants spécialement conçus. Ils sont généralement fabriqués à partir de métaux biocompatibles tels que le nitinol et présentent une conception pliable. Les dispositifs sont avancés dans le corps au moyen d’un cathéter et, placés sur l’ASD, permettent la fermeture de l’orifice.
Structure des dispositifs et principe de fonctionnement
Ces dispositifs sont généralement composés de deux disques. Lorsque ces disques sont amenés sur l’ASD par cathéter, ils s’ouvrent et se placent de chaque côté de l’orifice, empêchant ainsi le flux sanguin. Avec le temps, le corps entoure ce dispositif et permet son intégration avec le tissu naturel du cœur. Les dispositifs sont conçus de manière à ne pas endommager le tissu cardiaque et restent de façon permanente dans le corps.
Processus d’application des dispositifs
- Préparation : Le patient subit un examen détaillé avant la procédure et les examens d’imagerie nécessaires sont réalisés.
- Anesthésie : Une anesthésie locale et une sédation sont généralement suffisantes. L’anesthésie générale est rarement utilisée.
- Accès vasculaire : Une petite incision est réalisée dans l’artère ou la veine fémorale au niveau de l’aine, et une fine gaine (sheath) y est introduite.
- Mise en place du cathéter : Au moyen de cette gaine, un cathéter spécial est avancé jusqu’à l’ASD. La position du cathéter est surveillée en continu par des méthodes d’imagerie telles que l’échocardiographie ou la fluoroscopie.
- Mesure du défaut : La taille et la forme de l’ASD sont mesurées avec précision.
- Sélection et mise en place du dispositif : Un dispositif de fermeture de l’ASD adapté aux mesures est choisi. Le dispositif, replié à l’extrémité du cathéter, est amené sur l’ASD. Une fois qu’il est confirmé que le dispositif est dans la bonne position, il est lentement déployé et mis en place.
- Contrôle : Après la mise en place du dispositif, il est vérifié que le flux sanguin est complètement interrompu et que le dispositif est stable.
- Retrait de la gaine : La gaine est retirée et une pression est appliquée sur la zone d’accès afin d’arrêter le saignement.
Différents dispositifs de fermeture de l’ASD
Il existe sur le marché divers dispositifs de fermeture de l’ASD proposés par différents fabricants. En voici quelques-uns :
- A-Seed (Lifetech) : dispositif en forme de disque conçu spécialement pour les ASD secundum.
- M-Closer (Lifetech) : option adaptée à une large gamme d’ASD, pouvant être produite en différentes tailles et formes.
- Cardio-SEAL (NMT Medical) : ce dispositif est également largement utilisé dans la fermeture des ASD secundum.
- AMPLATZER Septal Occluder (St. Jude Medical/Abbott) : dispositif fiable utilisé depuis de nombreuses années dans le domaine de la fermeture de l’ASD.
Chacun de ces dispositifs peut avoir ses propres avantages et techniques d’application. Le dispositif à utiliser est déterminé par le médecin en fonction de l’anatomie du patient et des caractéristiques du défaut.
Avantages de la fermeture percutanée de l’ASD
Les méthodes de fermeture de l’ASD sans chirurgie présentent de nombreux avantages importants par rapport à la chirurgie traditionnelle :
- Moins invasive : il n’est pas nécessaire de recourir à une chirurgie à cœur ouvert, ce qui signifie moins de lésions tissulaires.
- Récupération plus rapide : les patients peuvent généralement sortir le jour même ou le lendemain. Le délai de retour à l’activité physique est beaucoup plus court.
- Moins de douleur : en l’absence d’incisions chirurgicales, le niveau de douleur est plus faible.
- Moins de risque d’infection : en l’absence de champ chirurgical, le risque d’infection diminue nettement.
- Avantages esthétiques : aucune grande cicatrice d’incision ne reste sur la cage thoracique.
- Coût plus faible : à long terme, le rapport coût-efficacité peut s’améliorer grâce à une durée d’hospitalisation plus courte et à une diminution des complications.
- Suffisance de l’anesthésie locale : dans la plupart des cas, une anesthésie générale n’est pas nécessaire.
Inconvénients et risques de la fermeture percutanée de l’ASD
Comme pour toute procédure médicale, les méthodes de fermeture de l’ASD sans chirurgie présentent également des risques et des inconvénients potentiels :
- Thrombus sur le dispositif : bien que rare, un caillot sanguin peut se former à la surface du dispositif. Cette situation peut entraîner un accident vasculaire cérébral ou d’autres événements emboliques. Les patients peuvent devoir utiliser des médicaments anticoagulants pendant une certaine période après la procédure.
- Déplacement du dispositif : dans de très rares cas, le dispositif peut se déplacer après sa mise en place. Cette situation peut nécessiter une intervention supplémentaire.
- Fermeture incomplète du défaut du septum interauriculaire (shunt résiduel) : malgré la mise en place du dispositif, une petite quantité de fuite sanguine peut persister. Cela est généralement sans importance clinique, mais peut, dans certains cas, nécessiter un suivi.
- Risque d’endocardite : la présence du dispositif peut théoriquement augmenter le risque d’endocardite infectieuse (infection des valves cardiaques). C’est pourquoi il est recommandé aux patients de respecter les règles d’hygiène et de consulter un médecin en cas de signes d’infection.
- Blocs de conduction atrio-ventriculaires : bien que rare, la position du dispositif peut affecter les voies de conduction et provoquer des blocs temporaires ou permanents.
- Complications liées à la gaine de gros vaisseau : des complications telles qu’un saignement, un hématome (accumulation de sang) ou un faux anévrisme peuvent être observées dans le vaisseau d’accès.
- Inadéquation anatomique : tous les patients atteints d’ASD ne sont pas adaptés à une fermeture percutanée. Des facteurs tels que la taille du défaut, sa localisation ou la structure vasculaire du patient peuvent empêcher l’application de cette méthode.
Taux de complications
Les taux de complications de la fermeture percutanée de l’ASD sont assez faibles. Les taux de réussite sont généralement supérieurs à 95 %. Les complications majeures (accident vasculaire cérébral, décès, saignement important, etc.) sont observées dans moins de 1 % des cas. Ces taux peuvent varier selon l’expérience du centre où l’intervention est réalisée et la technologie utilisée. Par exemple, une méta-analyse réalisée en 2018 a montré que le taux global de réussite de la fermeture percutanée de l’ASD était de 97,6 % et que le taux de complications graves était de 0,7 % (Source : Journal of the American College of Cardiology).
Qui est candidat à une fermeture de l’ASD sans chirurgie ?
La méthode de fermeture de l’ASD sans chirurgie est une option thérapeutique idéale pour les patients répondant à certains critères. Ces candidats sont généralement les suivants :
- Patients présentant un ASD secundum : les méthodes percutanées sont les plus efficaces dans la fermeture des ASD secundum.
- Patients symptomatiques : ASD provoquant des symptômes tels que l’essoufflement, la fatigue ou les palpitations.
- Défauts hémodynamiquement significatifs : ASD augmentant la charge de travail du cœur et provoquant une dilatation des cavités cardiaques droites.
- Patients présentant un risque chirurgical : patients âgés, présentant une maladie pulmonaire sévère associée ou d’autres affections chroniques, et présentant un risque élevé pour une chirurgie à cœur ouvert.
- Patients anatomiquement adaptés : patients chez qui la taille, la forme et la structure des bords du défaut sont adaptées à la mise en place percutanée d’un dispositif.
Quels types d’ASD peuvent être fermés par des méthodes percutanées ?
Les méthodes percutanées sont principalement utilisées pour la fermeture des ASD secundum. Comme ce type d’ASD se situe dans la partie moyenne du septum, il offre une zone appropriée pour la mise en place du dispositif. Les autres types d’ASD, tels que l’ASD primum, l’ASD du sinus veineux et l’ASD du sinus coronaire, nécessitent généralement une intervention chirurgicale. Cependant, avec les progrès technologiques, les recherches se poursuivent également sur la fermeture percutanée de ces types à l’aide de certains dispositifs spécialement conçus.
Y a-t-il une limite d’âge ?
Il n’existe pas de limite d’âge précise pour la fermeture de l’ASD sans chirurgie. La méthode peut être appliquée avec succès aussi bien chez les nourrissons que chez les personnes âgées. Toutefois, chez les nourrissons et les jeunes enfants, la taille du dispositif et l’état général du patient sont pris en compte. En général, chez les enfants, la décision de fermer l’ASD est prise en fonction de la taille du défaut et des symptômes du patient. Chez les adultes, elle peut être privilégiée en priorité chez les patients à haut risque chirurgical ou qui refusent la chirurgie.
Processus avant et après la fermeture de l’ASD sans chirurgie
Évaluation avant la procédure
Avant la procédure, une évaluation cardiologique détaillée du patient est effectuée. Cette évaluation comprend les éléments suivants :
- Antécédents médicaux et examen physique : l’état de santé général, les maladies existantes et les plaintes du patient sont examinés.
- Échocardiographie (ECHO) : la localisation, la taille, la structure des bords et l’importance hémodynamique de l’ASD sont déterminées.
- Électrocardiographie (ECG) : le rythme cardiaque et les éventuelles anomalies électriques sont évalués.
- Radiographie thoracique et analyses sanguines : elles permettent d’obtenir des informations sur l’état de santé général.
- Autres méthodes d’imagerie si nécessaire : des examens complémentaires tels que l’ETO, l’IRM ou la TDM peuvent être demandés.
Pendant la procédure
La procédure est généralement réalisée en laboratoire de cardiologie interventionnelle, dans des conditions stériles. Le médecin applique une anesthésie locale et une sédation selon l’état du patient. La durée de la procédure est en moyenne de 30 à 60 minutes. Pendant la procédure, les signes vitaux du patient (pouls, tension artérielle, saturation en oxygène) sont surveillés en continu.
Soins et suivi après la procédure
Après la procédure, les patients sont généralement maintenus en observation pendant plusieurs heures. Ils sortent généralement le jour même ou le lendemain. Les points auxquels il faut faire attention après la sortie sont les suivants :
- Repos : il convient d’éviter les activités physiques intenses pendant les premiers jours.
- Traitement médicamenteux : les médicaments anticoagulants recommandés par le médecin (comme l’aspirine, le clopidogrel) doivent être utilisés régulièrement. Ces médicaments sont importants pour prévenir la formation de caillots sur le dispositif.
- Soins de la plaie : la plaie au niveau de la zone d’accès doit être maintenue propre et les signes d’infection doivent être surveillés.
- Rendez-vous de contrôle : après la procédure, un contrôle médical est effectué à intervalles déterminés (généralement au 1er, 3e, 6e et 12e mois). Lors de ces contrôles, l’état du dispositif et la fermeture complète ou non de l’ASD sont évalués par échocardiographie.
- Soins dentaires : afin de réduire le risque d’endocardite infectieuse, il est recommandé de consulter votre médecin avant les soins dentaires invasifs et de recevoir la prophylaxie antibiotique nécessaire.
L’avenir de la fermeture de l’ASD sans chirurgie
Les méthodes de fermeture de l’ASD sans chirurgie ont permis une avancée importante dans le domaine de la cardiologie. À l’avenir, des développements encore plus importants sont attendus dans ce domaine :
- Conceptions de dispositifs plus avancées : des dispositifs plus compatibles, plus sûrs et plus faciles à mettre en place seront développés pour différents types d’ASD.
- Dispositifs biodégradables : à l’avenir, on vise le développement de dispositifs non permanents dans le corps et résorbables avec le temps.
- Applicabilité à un groupe plus large de patients : les recherches se poursuivent afin que les types d’ASD nécessitant actuellement une chirurgie puissent également être traités par des méthodes percutanées.
- Applications d’intelligence artificielle et de robotique : l’intégration de systèmes d’imagerie assistés par intelligence artificielle et de systèmes de chirurgie robotique peut être envisagée afin d’augmenter la précision pendant la procédure et de réduire les complications.
Questions fréquemment posées
La fermeture de l’ASD sans chirurgie est généralement appliquée dans les défauts du septum interauriculaire de type secundum. La taille de l’orifice, la suffisance des tissus marginaux et la structure cardiaque sont déterminantes pour la procédure. En cas de défauts très volumineux ou d’anatomie non adaptée, la chirurgie peut être préférée.
La fermeture de l’ASD sans chirurgie est réalisée au moyen d’un fin cathéter introduit par l’aine. Le dispositif spécial de fermeture est placé de part et d’autre de l’orifice dans le cœur, s’ouvre comme un parapluie et ferme l’orifice. La procédure est généralement réalisée sous angiographie et échocardiographie.
Après une fermeture de l’ASD sans chirurgie, un caillot peut rarement se former sur le dispositif. C’est pourquoi des médicaments anticoagulants sont utilisés pendant une certaine période après la procédure et des contrôles réguliers sont réalisés. Avec un suivi approprié, le risque est assez faible.
La fermeture de l’ASD sans chirurgie peut être recommandée durant l’enfance en cas d’augmentation du volume cardiaque, d’infections fréquentes ou de diminution de la capacité à l’effort. Une intervention précoce réduit le risque d’insuffisance cardiaque et de troubles du rythme pouvant se développer ultérieurement.
Chez les patients chez qui une fermeture de l’ASD sans chirurgie n’est pas réalisée, une augmentation de la pression pulmonaire, une augmentation du volume cardiaque, des troubles du rythme et une insuffisance cardiaque peuvent se développer avec le temps. À long terme, la qualité de vie peut diminuer et de graves problèmes cardiaques peuvent apparaître.
Après une fermeture de l’ASD sans chirurgie, les patients sortent généralement de l’hôpital dans un délai de 1 à 2 jours. Le retour à la vie quotidienne est possible en quelques jours. Les exercices intenses doivent cependant être évités pendant la durée recommandée par le médecin.
La fermeture de l’ASD sans chirurgie peut également être appliquée en toute sécurité chez les patients adultes. Cependant, dans les cas restés longtemps sans traitement, une évaluation détaillée est nécessaire s’il existe une pression pulmonaire élevée. Chez les patients appropriés, le taux de réussite est assez élevé.
La fermeture de l’ASD sans chirurgie réduit la charge cardiaque liée à l’augmentation du volume sanguin pendant la grossesse. La réalisation de la fermeture avant la grossesse réduit considérablement le risque de troubles du rythme et d’insuffisance cardiaque chez la future mère.
Après une fermeture de l’ASD sans chirurgie, les activités intenses ne sont pas recommandées pendant les premières semaines. Si les contrôles sont normaux, la plupart des patients peuvent faire du sport avec le temps. Pour les sportifs professionnels, une évaluation cardiologique est importante.
La fermeture de l’ASD sans chirurgie assure un taux de réussite supérieur à 95 % chez les patients appropriés. Le dispositif s’intègre avec le temps au tissu cardiaque et offre une solution permanente. Les résultats à long terme sont généralement très satisfaisants et la qualité de vie augmente.